| Opis |
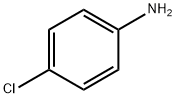
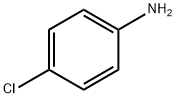
p-chloroanilina, 1-amino-4- chlorobenzen, jest krystalicznym ciałem stałym o barwie białej do jasnobursztynowej w temperaturze pokojowej. Jest stosowany jako półprodukt do pestycydów, farmaceutyków, pigmentów i barwników. Produkcja jest podobna do produkcji m-chloroaniliny. |
| Właściwości chemiczne |
4-Chloroanilina to bezbarwna do lekko bursztynowej krystaliczna substancja stała o łagodnym aromatycznym zapachu. Jest rozpuszczalny w gorącej wodzie i rozpuszczalnikach organicznych. 4-Chloroanilina ma umiarkowaną prężność par i współczynnik podziału n-oktanol/woda. Rozkłada się pod wpływem światła i powietrza oraz w podwyższonej temperaturze. |
| Właściwości fizyczne |
Żółtawobiała substancja stała o łagodnym, słodkawym zapachu. Stężenie progowe zapachu wynosi 287 ppm (cytat, Keith i Walters, 1992). |
| Używa |
4-Chloroanilina jest ważnym surowcem do produkcji chemikaliów rolniczych, barwników i pigmentów azowych, kosmetyków i produktów farmaceutycznych. Stosuje się go jako półprodukt do produkcji chromoforu AS-LB, a także w półproduktach farmaceutycznych, takich jak chlordiazepoksyd i nalewka fena. Jest także półproduktem dla herbicydu Anilofos, insektycydu chlorbenzuronu i regulatora wzrostu roślin Inabenfide. |
| Definicja |
ChEBI: 4-chloroanilina to chloroanilina, w której atom chloru znajduje się w pozycji para względem grupy aminowej aniliny. Jest chloroaniliną i członkiem monochlorobenzenów. |
| Aplikacja |
4-Chloroanilina to ważny element budulcowy stosowany w przemyśle chemicznym do produkcji leków i barwników. Niektóre leki benzodiazepinowe do produkcji wykorzystują 4-chloroanilinę. |
| Przygotowanie |
synteza 4-chloroaniliny: jako surowiec stosuje się p-chloronitrobenzen, nikiel Raneya stosuje się jako katalizator, etanol stosuje się jako rozpuszczalnik, temperatura reakcji wynosi 50-70 stopnia, ciśnienie uwodornienia wynosi 3.{{4} },55 MPa i średnim pH=5-6, przeprowadzić reakcję katalitycznego uwodornienia w celu otrzymania 4-chloroaniliny. |
| Odniesienia do syntezy |
Dziennik Amerykańskiego Towarzystwa Chemicznego, 99, s. 10-10. 98, 1977DOI:10.1021/ja00443a018
Synteza, s. 13 48, 1987DOI: 10.1055/s-1987-27838 |
| Ogólny opis |
P-chloroanilina ma postać białego lub bladożółtego ciała stałego. Temperatura topnienia 69,5 stopnia. |
| Reakcje powietrza i wody |
Nierozpuszczalny w zimnej wodzie. Rozpuszczalny w gorącej wodzie [Hawley]. |
| Profil reaktywności |
4-Chloroanilina jest niezgodna ze środkami utleniającymi. Niekompatybilny także z kwasami, chlorkami kwasowymi, bezwodnikami kwasowymi i chloromrówczanami. Podlega rozkładowi egzotermicznemu podczas destylacji w wysokiej temperaturze. Niekompatybilny z kwasem azotawym. |
| Zaryzykować |
Działa toksycznie przez drogi oddechowe i połknięcie. Możliwy czynnik rakotwórczy. |
| Zagrożenie dla zdrowia |
Wdychanie lub połknięcie powoduje niebieskawe zabarwienie paznokci, warg i uszu, co wskazuje na sinicę; ból głowy, senność i nudności, a następnie utrata przytomności. Ciecz może wchłaniać się przez skórę i powodować podobne objawy. Kontakt z oczami powoduje podrażnienie. |
| Zagrożenie pożarowe |
Szczególne zagrożenia związane z produktami spalania: Podczas pożaru mogą tworzyć się drażniący i toksyczny chlorowodór i tlenki azotu. |
| Palność i wybuchowość |
Zapalny |
| Profil bezpieczeństwa |
Potwierdzony czynnik rakotwórczy na podstawie eksperymentalnych danych dotyczących nowotworzenia i nowotworzenia. Trucizna po spożyciu, wdychaniu, kontakcie przez skórę, podskórnie i dożylnie. Substancja silnie drażniąca skórę i oczy. Zgłoszono dane dotyczące mutacji. Po podgrzaniu do rozkładu wydziela toksyczne opary Cland NOx. Zobacz także BARWNIKI ANILINOWE |
| Los środowiska |
Biologiczny.W środowisku beztlenowym bakterie Paracoccus sp. przekształcił 4- chloroanilinę w 1,3-bis(p-chlorofenylo)triazen i 4-chloroacetanilid z wydajnością produktu odpowiednio 80 i 5% (Minard i in., 1977). W eksperymencie polowym [14C]4-chloroanilinę nałożono na glebę na głębokość 10 cm. Po 20 tygodniach w glebie odzyskano 32,4% zastosowanej ilości. Zidentyfikowane metabolity obejmują 4-chloroformanilid, 4-chloroacetanilid, 4-chloronitrobenzen, 4- chloronitrozobenzen, 4,4′-dichloroazoksybenzen i 4,4′-dichloroazobenzen (Freitag i in. , 1984).
Gleba.4-Chloroanilina wiąże się kowalencyjnie z substancjami humusowymi w glebie, tworząc struktury chinoidalne, po których następuje utlenianie, w wyniku czego powstaje pierścień chinoidowy podstawiony azotem. Dla jednego związku humusowego określono okres półtrwania reakcji wynoszący 13 minut (Parris, 1980). Katechol, monomer kwasu humusowego, poddał się reakcji z 4-chloroaniliną, w wyniku czego otrzymano 4,5-bis(4-chlorofenyloamino)-3,5-cykloheksadien-1, 2-dion (Adrian i in., 1989).
Fotolityczny.Under artificial sunlight, river water containing 2–5 ppm 4-chloroaniline photodegraded to 4-aminophenol and unidentified polymers (Mansour et al., 1989). Photooxidation of 4-chloroaniline (100 μM) in air-saturated water using UV light (λ >290 nm) produced 4-chloronitrobenzene and 4-chloronitrosobenzene. About 6 h later, 4-chloroaniline completely reacted leaving dark purple condensation products (Miller and Crosby, 1983). In a similar study, irradiation of an aqueous solution in the range of 290–350 nm resulted in the formation of the intermediate 4-iminocyclohexa-2,5-dienylidene (Othmen et al., 2000). A carbon dioxide yield of 27.7% was achieved when 4-chloroaniline adsorbed on silica gel was irradiated with light (λ >290 nm) przez 17 godzin (Freitag i in., 1985).
Stała szybkości wynosząca 8,3 x 10-11cm3/molekułę?s podano dla reakcji w fazie gazowej 4- chloroaniliny i rodników OH w powietrzu (Wahner i Zetzsch, 1983).
Chemiczne/fizyczne.4-Chloroanilina nie ulega hydrolizie w rozsądnym stopniu (Kollig, 1993).
Pizzigalo i in. (1998) badali reakcję 4-chloroaniliny z tlenkiem żelaza i dwiema postaciami dwutlenku manganu [birnessyt (δ-MnO2) i piroluzyt (MnO2)] w zakresie pH 4–8 w temperaturze 25 stopni. Szybkość reakcji 4-chloroaniliny była rzędu birnessyt > piroluzyt > tlenek żelaza. Przy pH 4,0 reakcja z birnessytem była tak szybka, że nie można było jej określić. Okresy półtrwania w reakcji 4-chloroaniliny z piroluzytem i tlenkiem żelaza wynosiły odpowiednio 383 i 746 minut. Szybkość reakcji zmniejszała się wraz ze wzrostem pH. Jedynymi związkami utleniającymi zidentyfikowanymi metodą GC/MS były 4,4′-dichloroazobenzen i 4-chloro-4′-hydroksydifenyloamina. |
| Metody oczyszczania |
Krystalizować anilinę z MeOH, eteru naftowego (b 30-60o) lub 50% wodnego roztworu EtOH, następnie *benzenu/eteru naftowego (b 60-70o), a następnie wysuszyć w eksykatorze próżniowym. Można go destylować pod próżnią (b 75-77o/3 mm). Sublimuje w bardzo wysokiej próżni. Octan krystalizuje z wodnego MeOH (m 178o, 180o) lub EtOH lub AcOH (m 173-174o) i ma b 331,3o/760 mm. [Beilstein 12 III 1325, 12 IV 1116.] |